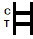Abschlussball schneller Test
Beabsichtigte Verwendung
Der Strongstep®Der Prom-Test ist ein visuell interpretierter, qualitativer immunochromatographischer Test zum Nachweis von IGFBP-1 aus Fruchtwasser in Vaginalsekreten während der Schwangerschaft. Der Test dient für den professionellen Gebrauch, um das Bruch von fetalen Membranen (ROM) bei schwangeren Frauen zu diagnostizieren.
EINFÜHRUNG
Die Konzentration von IGFBP-1 (Insulin-ähnlicher Wachstumsfaktor-Bindungsprotein-1) in Fruchtwasser ist 100- bis 1000-mal höher als im mütterlichen Serum. IGFBP-1 ist normalerweise nicht in der Vagina vorhanden, aber nach dem Bruch von fetalen Membranen ist Fruchtwasser mit einer hohen Konzentration von IGFBP-1-Mischungen mit Vaginalsekreten. Bei einem Prom -Test für den Stronstp® wird ein Probe der Vaginalsekretion mit einem sterilen Polyester -Tupfer durchgeführt und die Probe in die Lösung der Probenextraktion extrahiert. Das Vorhandensein von IGFBP-1 in der Lösung wird unter Verwendung eines schnellen Testgeräts erkannt.
PRINZIP
Der Strongstep®Der Prom -Test verwendet die immunochromatographische Farb -Kapillarfluss -Technologie. Das Testverfahren erfordert die Solubilisierung von IGFBP-1 aus einem Vaginalabstrich, indem der Tupfer im Probenpuffer gemischt wird. Dann wird der gemischte Probenpuffer zur Testkassettenprobe -Probe -Probe hinzugefügt und die Mischung entlang der Membranoberfläche migriert. Wenn IGFBP-1 in der Probe vorhanden ist, bildet es einen Komplex mit dem primären Anti-IGFBP-1-Antikörper-Antikörper, der an farbige Partikel konjugiert ist. Der Komplex wird dann durch einen zweiten Anti-IGFBP-1-Antikörper gebunden, der mit der Nitrocellulosemembran beschichtet ist. Das Erscheinungsbild einer sichtbaren Testlinie zusammen mit der Kontrolllinie zeigt ein positives Ergebnis.
Kit -Komponenten
| 20 Individuell packED -Testgeräte | Jedes Gerät enthält einen Streifen mit farbigen Konjugaten und reaktiven Reagenzien, die in den entsprechenden Regionen vorgeschoben wurden. |
| 2ExtraktionPufferfläschchen | 0,1 M Phosphat gepuffert Kochsalzlösung (PBS) und 0,02% Natriumazid. |
| 1 Positive Kontrolle Tupfer (nur auf Anfrage) | IGFBP-1 und Natriumazid enthalten. Für externe Kontrolle. |
| 1 Negativkontrollabstrich (nur auf Anfrage) | Nicht IGFBP-1 enthalten. Für externe Kontrolle. |
| 20 Extraktionsrohre | Für die Verwendung von Proben vorbereitet. |
| 1 Arbeitsplatz | Stellen Sie Pufferfläschchen und Röhrchen fest. |
| 1 Paketeinsatz | Für Betriebsanweisung. |
Materialien erforderlich, aber nicht bereitgestellt
| Timer | Für die Timing -Verwendung. |
VORSICHTSMASSNAHMEN
■ Nur für professionelle In -vitro -diagnostische Verwendung.
■ Verwenden Sie nicht nach dem auf dem Paket angegebenen Ablaufdatum. Verwenden Sie den Test nicht, wenn sein Folienbeutel beschädigt ist. Wiederverwenden Sie keine Tests.
■ Dieses Kit enthält Produkte tierischer Herkunft. Zertifizierte Kenntnisse über den Ursprung und/oder den Sanitärzustand der Tiere garantieren nicht vollständig das Fehlen übergreifbarer pathogener Wirkstoffe. Es wird daher empfohlen, diese Produkte als potenziell ansteckend behandelt zu werden und die üblichen Sicherheitsvorkehrungen zu beobachten (nicht einnehmen oder einatmen).
■ Vermeiden Sie die Querkontamination von Proben mit einem neuen Probensammlungsbehälter für jedes erhaltene Probe.
■ Lesen Sie das gesamte Verfahren sorgfältig durch, bevor Sie Tests durchführen.
■ In der Gegend, in der die Exemplare und Kits behandelt werden, nicht essen, trinken oder rauchen. Behandeln Sie alle Exemplare so, als ob sie Infektionsmittel enthalten. Beobachten Sie festgelegte Vorsichtsmaßnahmen gegen mikrobiologische Gefahren während des gesamten Verfahrens und befolgen Sie die Standardverfahren für die ordnungsgemäße Entsorgung von Proben. Tragen Sie Schutzkleidung wie Labormäntel, Einweghandschuhe und Augenschutz, wenn Proben untersucht werden.
■ Verankern Sie oder mischen Sie Reagenzien nicht aus verschiedenen Lose. Mischen Sie keine Lösungsflaschenkappen.
■ Feuchtigkeit und Temperatur können die Ergebnisse nachteilig beeinflussen.
■ Wenn das Assay -Verfahren abgeschlossen ist, entsorgen Sie die Tupfer sorgfältig, nachdem Sie sie mindestens 20 Minuten bei 121 ° C autoklavieren. Alternativ können sie vor der Entsorgung eine Stunde lang mit 0,5% Natriumhypochlorid (oder Haushaltsbleichmittel) behandelt werden. Die verwendeten Testmaterialien sollten gemäß den Vorschriften lokaler, staatlicher und/oder föderaler Bestimmungen verworfen werden.
■ Verwenden Sie keine Zytologiebürsten mit schwangeren Patienten.
Speicherung und Stabilität
■ Das Kit sollte bis zum Ablaufdatum auf dem versiegelten Beutel bei 2-30 ° C gelagert werden.
■ Der Test muss bis zur Verwendung im versiegelten Beutel bleiben.
■ NICHT einfrieren.
■ Für die Schutzkomponenten in diesem Kit vor Kontamination sollten sich um Sorgen befassen. Verwenden Sie nicht, wenn es Hinweise auf mikrobielle Kontamination oder Niederschlag gibt. Die biologische Kontamination von Abgabeausrüstungen, Behältern oder Reagenzien kann zu falschen Ergebnissen führen.
Sammlung und Speicherung von Proben
Verwenden Sie nur Dacron oder Rayon mit sterilen Tupfer mit Plastikwellen. Es wird empfohlen, den vom Kits -Hersteller gelieferten Tupfer zu verwenden (die Tupfer sind in diesem Kit nicht enthalten. Für die Bestellinformationen wenden Sie sich bitte an den Hersteller oder den örtlichen Händler, die Kataloge -Nummer beträgt 207000). Tupfer von anderen Lieferanten wurden nicht validiert. Es werden keine Tupfer mit Baumwollspitzen oder Holzwellen empfohlen.
■ Eine Probe wird unter Verwendung eines sterilen Polyesterabstrichs erhalten. Die Probe sollte vor der Durchführung digitaler Untersuchungen und/oder transvaginaler Ultraschall gesammelt werden. Achten Sie darauf, nichts mit dem Tupfer zu berühren, bevor Sie die Probe nehmen. Setzen Sie die Tupferspitze vorsichtig in die Vagina in Richtung des hinteren Fornix ein, bis der Widerstand erfüllt ist. Alternativ kann die Probe während einer sterilen Spekulumuntersuchung aus dem hinteren Fornix entnommen werden. Der Tupfer sollte 10-15 Sekunden lang in der Vagina gelassen werden, damit er die Vaginalsekretion absorbiert. Ziehen Sie den Tupfer vorsichtig heraus !.
■ Legen Sie den Tupfer auf das Extraktionsrohr, wenn der Test sofort durchgeführt werden kann. Wenn sofortige Tests nicht möglich sind, sollten die Patientenproben zur Lagerung oder zum Transport in ein Trockentransportrohr gelegt werden. Die Tupfer können 24 Stunden bei Raumtemperatur (15-30 ° C) oder 1 Woche bei 4 ° C oder nicht mehr als 6 Monaten bei -20 ° C gelagert werden. Alle Proben sollten vor dem Testen eine Raumtemperatur von 15 bis 30 ° C erreichen.
VERFAHREN
Testen, Proben, Puffer und/oder Steuerungen vor der Verwendung auf Raumtemperatur (15-30 ° C) bringen.
■ Legen Sie ein sauberes Extraktionsrohr in den angegebenen Bereich der Workstation. Fügen Sie 1 ml Extraktionspuffer zum Extraktionsrohr hinzu.
■ Legen Sie den Exemplarabstrich in die Röhre. Mischen Sie die Lösung energisch, indem Sie den Tupfer für den mindestens zehnmaligen Röhrchen mit Kraftgrad drehen (während eingetaucht). Die besten Ergebnisse werden erzielt, wenn die Probe in der Lösung energisch gemischt wird.
■ So viel Flüssigkeit wie möglich aus dem Tupfer ausdrücken, indem Sie die Seite des flexiblen Extraktionsrohrs beim Entfernen des Tupfes einklemmen. Mindestens 1/2 der Probenpufferlösung muss im Rohr verbleiben, damit eine angemessene Kapillarmigration auftritt. Legen Sie die Kappe auf das extrahierte Rohr.
Verwerfen Sie den Tupfer in einem geeigneten biologischen Abfallbehälter.
■ Die extrahierten Proben können 60 Minuten bei Raumtemperatur bleiben, ohne das Ergebnis des Tests zu beeinflussen.
■ Entfernen Sie den Test aus seinem versiegelten Beutel und legen Sie ihn auf eine saubere, ebene Oberfläche. Beschriften Sie das Gerät mit Patienten oder Kontrollidentifikation. Um ein bestes Ergebnis zu erzielen, sollte der Assay innerhalb einer Stunde durchgeführt werden.
■ Fügen Sie 3 Tropfen (ungefähr 100 µl) extrahierter Probe aus dem Extraktionsrohr in die Probe gut in der Testkassette hinzu.
Vermeiden Sie es, Luftblasen in den Proben -Brunnen zu fangen und lassen Sie keine Lösung im Beobachtungsfenster fallen.
Wenn der Test zu funktionieren beginnt, wird sich die Farbe über die Membran bewegen.
■ Warten Sie, bis die farbigen Bande (en) erscheint. Das Ergebnis sollte nach 5 Minuten gelesen werden. Interpretieren Sie das Ergebnis nicht nach 5 Minuten.
Verwendete Testrohre und Testkassetten in geeigneten biohazartigen Abfallbehälter.
NTRETATION DER ERGEBNISSE
| POSITIVERGEBNIS:
| Auf der Membran erscheinen zwei farbige Bänder. Eine Bande erscheint in der Kontrollregion (c) und eine andere Bande erscheint in der Testregion (T). |
| NEGATIVERGEBNIS:
| In der Kontrollregion (c) erscheint nur eine farbige Bande. In der Testregion (T) wird kein scheinbar farbiges Band erscheint. |
| UNGÜLTIGERGEBNIS:
| Kontrollband erscheint nicht. Die Ergebnisse eines Tests, der zur angegebenen Lesezeit kein Kontrollband erzeugt wurde, müssen verworfen werden. Bitte überprüfen Sie die Prozedur und wiederholen Sie dies mit einem neuen Test. Wenn das Problem bestehen bleibt, stellen Sie die Verwendung des Kits sofort ein und wenden Sie sich an Ihren örtlichen Händler. |
NOTIZ:
1. Die Intensität der Farbe im Testbereich (t) kann je nach Konzentration der in der Probe vorhandenen Konzentration der gezielten Substanzen variieren. Der Substanzenniveau kann jedoch nicht durch diesen qualitativen Test bestimmt werden.
2. Unzureichendes Probenvolumen, falsches Betriebsverfahren oder abgelaufene Tests sind die wahrscheinlichsten Gründe für den Versagen des Kontrollbandes.
QUALITÄTSKONTROLLE
■ Interne Verfahrenskontrollen sind im Test enthalten. Eine farbige Bande, die in der Kontrollregion (c) auftritt, wird als interne positive Verfahrenskontrolle angesehen. Es bestätigt ein ausreichendes Probenvolumen und die korrekte Verfahrenstechnik.
■ In den Kits können externe Verfahrenskontrollen (nur auf Anfrage) bereitgestellt werden, um sicherzustellen, dass die Tests ordnungsgemäß funktionieren. Außerdem können die Steuerelemente verwendet werden, um die ordnungsgemäße Leistung durch den Testoperator zu demonstrieren. Um einen positiven oder negativen Kontrolltest durchzuführen, führen Sie die Schritte im Abschnitt Testverfahren aus, der den Kontrollabstrich auf die gleiche Weise wie ein Probenabstrich behandelt.
Einschränkungen des Tests
1. Auf der Grundlage der Testergebnisse sollte keine quantitative Interpretation durchgeführt werden.
2. Verwenden Sie den Test nicht, wenn sein Aluminiumfolienbeutel oder die Dichtungen des Beutels nicht intakt sind.
3. Ein positiver Stronstp®Das Prom -Testergebnis, obwohl das Vorhandensein von Fruchtwasser in der Probe nachgewiesen wird, lokalisiert es nicht die Stelle des Bruchs.
4. Wie bei allen diagnostischen Tests müssen die Ergebnisse im Lichte anderer klinischer Befunde interpretiert werden.
5. Wenn die Fötalmembranen gebrochen wurden, aber die Lecknahme von Fruchtwasser-Flüssigkeit mehr als 12 Stunden vor der Einnahme der Probe eingestellt wurde, wurde IGFBP-1 möglicherweise durch Proteasen in der Vagina abgebaut und der Test kann ein negatives Ergebnis liefern.
Leistungseigenschaften
Tabelle: Strongstep®Prom -Test gegen einen anderen Marken -Prom -Test
|
Relative Empfindlichkeit: |
| Eine andere Marke |
| ||
| + | - | Gesamt | |||
| Starker®Abschlussball Prüfen | + | 63 | 3 | 66 | |
| - | 2 | 138 | 140 | ||
|
| 65 | 141 | 206 | ||
Analytische Empfindlichkeit
Die niedrigste nachweisbare Menge an IGFBP-1 in der extrahierten Probe beträgt 12,5 μg/l.
Störende Substanzen
Es muss darauf geachtet werden, die Anwendungs- oder Gebärmutterhalssekrete mit Schmiermittel, Seifen, Desinfektionsmitteln oder Cremes nicht zu kontaminieren. Schmiermittel oder Cremes können die Absorption der Probe am Applikator physisch beeinträchtigen. Seifen oder Desinfektionsmittel können die Antikörper-Antigen-Reaktion beeinträchtigen.
Potenzielle störende Substanzen wurden in Konzentrationen getestet, die in Cervicovaginalsekreten vernünftigerweise gefunden werden könnten. Die folgenden Substanzen störten den Assay nicht, wenn sie auf den angegebenen Ebenen getestet wurden.
| Substanz | Konzentration | Substanz | Konzentration |
| Ampicillin | 1,47 mg/ml | Prostaglandin F2 | 0,033 mg/ml |
| Erythromycin | 0,272 mg/ml | Prostaglandin E2 | 0,033 mg/ml |
| 3. Trimester mütterlicher Urin | 5% (Vol) | Monistatr (Miconazol) | 0,5 mg/ml |
| Oxytocin | 10 IU/ml | Indigo Carmine | 0,232 mg/ml |
| Terbutalin | 3,59 mg/ml | Gentamicin | 0,849 mg/ml |
| Dexamethason | 2,50 mg/ml | Betadiner Gel | 10 mg/ml |
| Mgso4•7H2O | 1,49 mg/ml | Betadiner Reiniger | 10 mg/ml |
| Ritodrine | 0,33 mg/ml | K-IR-Gelee | 62,5 mg/ml |
| Dermicidolr 2000 | 25,73 mg/ml |
Literaturreferenzen
Erdemoglu und Mungan T. Signifikanz der Nachweis von Insulin-ähnlichen Wachstumsfaktor-Bindungsprotein-1 in Cervicovaginalsekretionen: Vergleich mit Nitrazin-Test und Volumenbewertung des Fruchtwasserflüssigkeit. Acta Obstet Gynecol Scand (2004) 83: 622-626.
Kubota T und Takeuchi H. Bewertung des Insulin-ähnlichen Wachstumsfaktorbindungsproteins-1 als diagnostisches Instrument zum Bruch der Membranen. J Obstet Gynecol Res (1998) 24: 411-417.
Rutanen EM et al. Bewertung eines schnellen Strip-Tests für insulinartiges Wachstumsfaktor-Bindungsprotein-1 bei der Diagnose von gebrochenen fetalen Membranen. Clin Chim Acta (1996) 253: 91-101.
Rutanen EM, Pekonen F, Karkkainen T. Messung von Insulin-ähnlichen Wachstumsfaktor-Bindungsprotein-1 in zervikalen/vaginalen Sekreten: Vergleich mit der ROM-Check-Membran-Immunoassay bei der Diagnose gebrochener fetaler Membranen. Clin Chim Acta (1993) 214: 73-81.
Glossar von Symbolen
|
| Katalognummer |  | Temperaturbeschränkung |
 | Anweisungen zur Verwendung konsultieren |
| Stapelcode |
 | In -vitro -diagnostische Medizinprodukte |  | Benutzen von |
 | Hersteller |  | Enthält ausreichend für |
 | NICHT wiederverwenden |  | Autorisierter Vertreter in der europäischen Gemeinschaft |
 | CE markiert gemäß IVD Medical Devices Direktive 98/79/EC | ||