Strongstep-Systemgerät für SARS-CoV-2-Antigen-Schnelltest
Beabsichtigte Verwendung
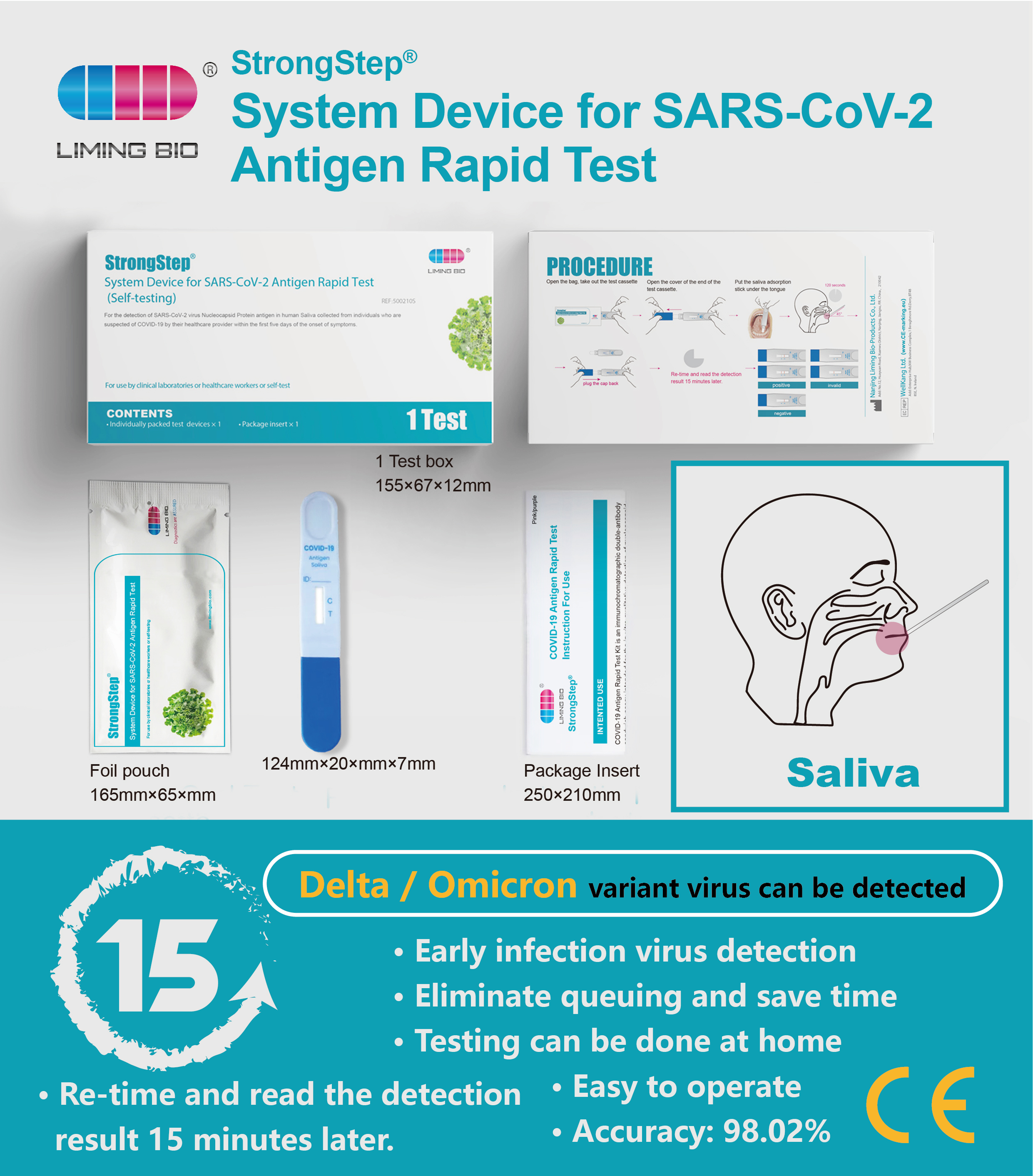
Das Strongstep®-Systemgerät für SARS-CoV-2-Antigen-Schnelltest verwendet die Immunochromatographie-Technologie, um das SARS-COV-2-Nucleocapsid-Antigen im menschlichen Speichel zu erkennen. Dieser Test ist nur einzelner Gebrauch und für SEI -Tests bestimmt. Es wird empfohlen, diesen Test innerhalb von 7 Tagen nach Beginn der Symptome zu verwenden. Es wird durch die klinische Leistungsbewertung gestützt.
EINFÜHRUNG
Die neuartigen Coronaviren gehören zur 0 Gattung. Covid-19 ist eine akute Infektionskrankheit der Atemwege. Menschen sind im Allgemeinen anfällig. Derzeit sind die vom neuartigen Coronavirus infizierten Patienten die Hauptinfektionsquelle, die auf der aktuellen epidemiologischen Untersuchung basiert. Die Inkubationszeit beträgt 1 bis 14 Tage, meist 3 bis 7 Tage. Die Hauptmanifestationen sind Fieber, Müdigkeit und trockener Husten. In einigen Fällen sind Nasenstaus, laufende Nase, Halsschmerzen, Myalgie und Durchfall zu finden.
PRINZIP
Das Strongstep®-Systemgerät für den SARS-CoV-2-Antigen-Test verwendet immunochromatographischen Test. Dieses Kit sammelt Speichelproben aus dem Speicheladsorptionsstock an der Vorderseite der Testkarte, und die Speichelproben treten unter Kapillarwirkung vor. Wenn die Probe ein SARS-CoV-2-N-Protein-Antigen enthält, wird es identifiziert und durch Antikörper gebunden, die auf der Latexoberfläche markiert werden, um einen Immunkomplex zu bilden. Wenn der gebildete Immunkomplex auf die Detektionslinie der Salpetersäure-Fasermembran wandert, um die gepackten Antikörper zu identifizieren und eine Fuchsia-Detektionslinie (T-Lins) zu bilden, die SARS-COV-2-Antigen-positives Antigen-positiv ist; Wenn die T-Linie keine Farbe zeigt, ist dies ein negatives Ergebnis. Eine weitere Linie auf der Salpetersäurefasermembran ist mit Streptavidin -Antikörpern als Qualitätskontrolllinie (C -Linie) gepackt, um einen wirksamen Testprozess anzuzeigen.
VORSICHTSMASSNAHMEN
• Dieses Kit dient nur zum In -vitro -diagnostischen Gebrauch.
• Dieses Kit kann von medizinischem oder nicht medizinischem Personal durch Befolgen der Betriebsanweisungen verabreicht werden.
• Lesen Sie die Anweisungen sorgfältig durch, bevor Sie den Test durchführen.
• Dieses Produkt enthält keine menschlichen Quellenmaterialien.
• Verwenden Sie den Kit -Inhalt nach dem Ablaufdatum nicht.
• Behandeln Sie alle Exemplare als potenziell ansteckend.
• Pipette Reagenz nicht durch Mund und kein Rauchen oder Essen während der Durchführung von Assays.
• Tragen Sie während des gesamten Verfahrens Handschuhe.
Speicherung und Stabilität
Die versiegelten Beutel im Testkit können für die Dauer der Haltbarkeit zwischen 2 und 30 ° C gelagert werden, wie auf dem Beutel angegeben.
Sammlung und Speicherung von Proben
Das beste Speichelproben sollte am Morgen nach dem Aufwachen gesammelt werden. Essen oder trinken Sie nicht 30 Minuten lang etwas, bevor Sie Ihre Speichelprobe sammeln. Tun Sie es, bevor Sie Kaffee trinken, Frühstück essen oder die Zähne putzen - oder warten Sie, bis Sie in den vorherigen 30 Minuten nichts mehr konsumiert haben.
VERFAHREN
Tests vor dem Gebrauch auf Raumtemperatur (15-30 ° C) bringen.
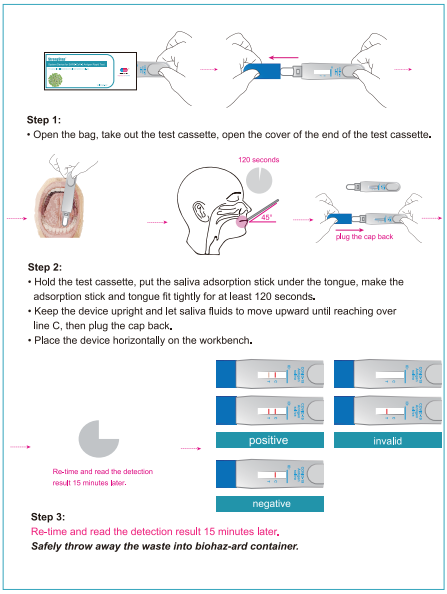
Schritt 1:
Öffnen Sie die Tasche, nehmen Sie das Testgerät heraus und öffnen Sie die Abdeckung des Testgeräts.
Schritt 2:
• Halten Sie die Lust auf Kassette, legen Sie den Speichel -Adsorptionsstift unter die Zunge, lassen Sie den Adsorptionsstab und die Zunge mindestens 120 Sekunden lang fest passen.
• Halten Sie das Gerät aufrecht und lassen Sie Speichelflüssigkeiten nach oben, bis sie über die Linie C greifen, und schließen Sie die Kappe zurück.
• Legen Sie das Gerät horizontal auf die Workbench.
Schritt 3:
Wiederzeit und lesen Sie die Erkennung 15 Minuten später erneut.
Werfen Sie den Abfall sicher in den Biohaz-Mardenbehälter weg.
QUALITÄTSKONTROLLE
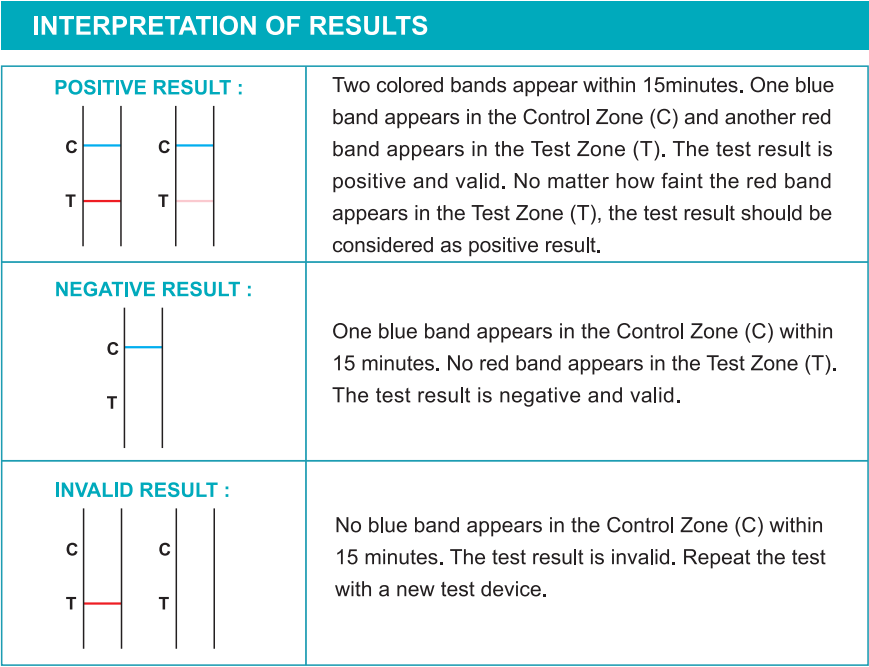
Interne Verfahrenskontrollen sind in den Test enthalten. Eine blaue Bande, die in der Kontrollregion (c) auftritt, wird als interne Verfahrenskontrolle angesehen. Es bestätigt ein ausreichendes Probenvolumen und die korrekte Verfahrenstechnik.
Einschränkungen des Tests
1. Das Kit soll für den qualitativen Nachweis von SARS-CoV-2-Antigenen aus Speichel verwendet werden.
2. Dieser Test erkennt sowohl lebensfähige (lebende) als auch nicht lebensfähige SARS-CoV-2. Die Testleistung hängt von der Menge an Virus (Antigen) in der Stichprobe ab und kann mit den Ergebnissen der Viruskultur korrelieren oder nicht, die an derselben Stichprobe durchgeführt werden.
3.. Ein negatives Testergebnis kann auftreten, wenn der Antigenniveau in einer Probe unter der Nachweisgrenze des Tests liegt oder wenn die Probe nicht ordnungsgemäß gesammelt oder transportiert wurde.
4. Die Nichteinhaltung des Testverfahrens kann die Testleistung nachteilig beeinflussen und/oder das Testergebnis ungültig machen.
5. Das Kit ist nur zum mutmaßlichen Screening gedacht. Negative Ergebnisse schließen keine SARS-CoV-2-Infektion aus und die Person, die nicht ansteckend ist. Wenn Symptome vorliegen, suchen Sie sofort weitere Tests.
6. Die Testergebnisse müssen mit der klinischen Anamnese, epidemiologischen Daten und anderen Daten korreliert werden, die dem Kliniker zur Bewertung des Patienten zur Verfügung stehen.
7. Positive Testergebnisse schließen keine Koinfektionen mit anderen Krankheitserregern aus und können nicht unbedingt feststellen, ob eine Person infektiös ist.
8. Negative Testergebnisse sollen bei anderen nicht-SARS-viralen oder bakteriellen Infektionen nicht regieren.
9. Negative Ergebnisse von Patienten mit Symptomen sollten als mutmaßlich behandelt und mit einem lokalen FDA -autorisierten molekularen Assay für das klinische Management, einschließlich der Infektionskontrolle, bestätigt werden.
10. Empfehlungen der Probenstabilität basieren auf Stabilitätsdaten aus Influenza-Tests und Leistung kann sich bei SARS-COV-2 unterscheiden. Benutzer sollten Exemplare nach der Probensammlung so schnell wie möglich testen.
11. Die Empfindlichkeit für den RT-PCR-Assay bei der Diagnose von COVID-199 beträgt nur 50% bis 80%, da die Empfindlichkeit des SASAR-COV-2-Antigen-Rapid-Testgeräts die Empfindlichkeit des Rapid-Testgeräts der Proben oder der Krankheitszeit in der Wiederherstellung der Erholung theoretisch ist niedriger wegen seiner Methodik.
12. Positive und negative Vorhersagewerte hängen stark von Prävalenzraten ab.
Positive Testergebnisse sind eher falsch positive Ergebnisse in Perioden mit wenig / ohne SARS-CoV-2-Aktivität, wenn die Prävalenz der Krankheit niedrig ist. FaLSE Negative Testergebnisse sind wahrscheinlicher, wenn die durch SARS-CoV-2 verursachte Prävalenz von Krankheiten hoch ist.
13. Monoklonale Antikörper können SARS-CoV-2-Influenzaviren, die sich in der Zielepitopregion mit geringfügigen Aminosäure-Veränderungen unterzogen oder mit weniger Empfindlichkeit nachweisen oder mit weniger Empfindlichkeit nachweisen.
14. Die Leistung dieses Tests wurde nicht für die Verwendung bei Patienten ohne Anzeichen von Anzeichen von Atemwegsinfektionen bewertet und die Leistung kann bei asymptomatischen Personen unterschiedlich sein.
15. Die Menge an Antigen in einer Probe kann mit zunehmendem Krankheitsdauer abnehmen.
Proben, die nach dem 7. Tag der Krankheit gesammelt wurden, sind im Vergleich zu einem RT-PCR-Assay mit größerer Wahrscheinlichkeit negativ.
Es ist bekannt, dass die Empfindlichkeit des Tests nach sieben Tagen des Einsetzens der Symptome im Vergleich zu einem RT-PCR-Assay abnimmt.
16. Es wird nicht empfohlen, in diesem Test Virus Transportation Media (VTM) -Probe zu verwenden. Wenn Kunden darauf bestehen, diesen Stichprobentyp zu verwenden, sollten sich die Kunden selbst validieren.
17. Häufige Tests sind erforderlich, um die Empfindlichkeit der Diagnose von Covid-19 zu erhöhen.
18. Kein Rückgang der Empfindlichkeit im Vergleich zum Wildtyp in Bezug auf die folgenden Varianten -B.1.1.7; B.1.351; B.1.2; B.1.1.28; B.1.617; B.1.1.529.
19. Positive Ergebnisse deuten darauf hin, dass in der genommenen Stichprobe virale Antigene festgestellt wurden. Bitte selbst querantinisch und informieren Sie Ihren Hausarzt unverzüglich und/oder Ihr örtliches Gesundheitsministerium gemäß den staatlichen Anforderungen.
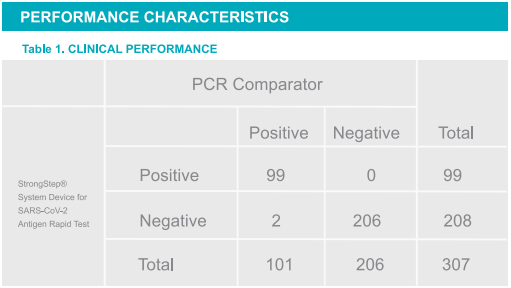
Positive prozentuale Übereinstimmung: (PPA) = 98,02%(93,03%~ 99,76%)*
Negative prozentuale Übereinstimmung: (NPA) = 100%(98,23%~ 100%)*
Gesamtfassungsrate = 98,76%
*95%Konfidenzintervall
Analytische Leistung
a) Erkennungsgrenze (LOD):
Die Erkennungsgrenze (LOD) des Tests wurde unter Verwendung von begrenzenden Verdünnungen von inaktiviertem SARS-CoV-2 bestimmt. Es handelt sich um eine Herstellung von SARS-bezogenen Coronavirus-2 (SARS-CoV-2), das in China CDC isoliert ist und durch β-Propiolakton inaktiviert wurde. Das Material wurde in einer TCID -Konzentration eingefroren50von 5,00 x 105/ml.
Um den SARS-COV-2 zu bestimmen, um den Assay bei der Verwendung direkter Speichel zu reflektieren. In dieser Studie wurde ungefähr 50 μl der Virusverdünnung mit der Speichel -negativen Probe versetzt.
Die LOD wurde in drei Schritten bestimmt:
1. LOD -Screening
10-fache Verdünnungen des inaktivierten Virus wurden in negativer Speichel vorgenommen und für jede Studie wie oben beschrieben verarbeitet. Diese Verdünnungen wurden dreifach getestet. Die Konzentration, die 3 von 3 Positiven demonstriert, wurde für den Erkenntnis des LOD -Bereichs ausgewählt.
2. Erkenntnis
Es wurden fünf (5) Verdünnungen der TCID verdoppelt50von 5,00 x 102/ML -Konzentration in negativen Speichel, die für die oben beschriebene Studie für die Studie verarbeitet wurden. Diese Verdünnungen wurden dreifach getestet. Die Konzentration, die 3 von 3 Positiven zeigt, wurde zur Bestätigung der LOD ausgewählt.
3.. LOD -Bestätigung
Die Konzentration tcid50von 2,50 x 102/ML -Verdünnung wurde auf insgesamt zwanzig (20) Ergebnisse getestet. Mindestens neunzehn (19) von zwanzig (20) Ergebnissen waren positiv.
Abschluss:
Basierend auf diesen Tests wurde die Konzentration als:
LOD: TCID502,50 x 102/ml
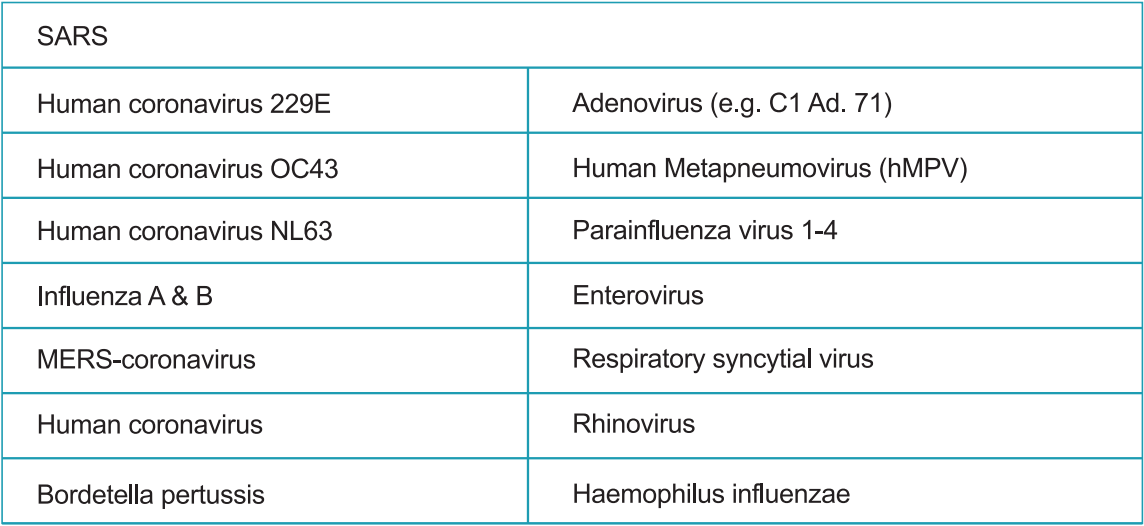
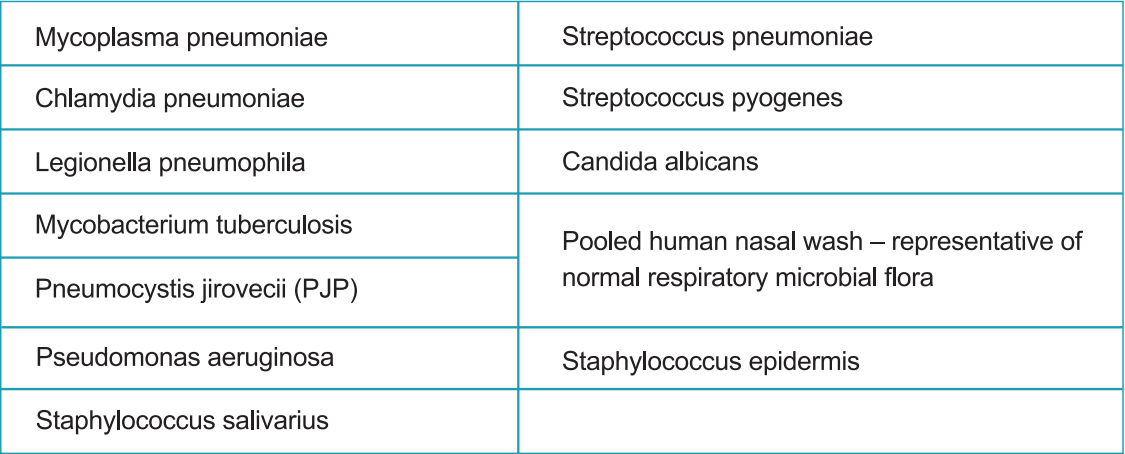
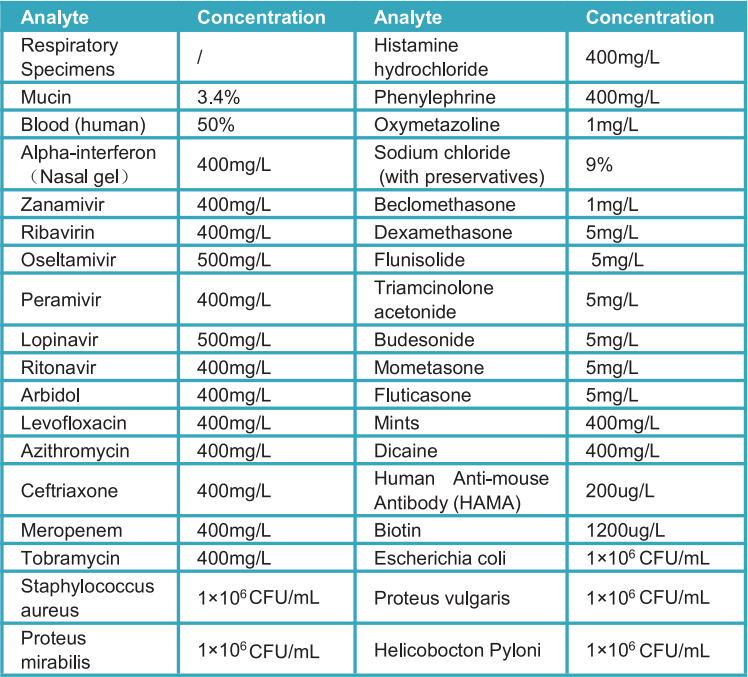
b) Kreuzreaktivität:
Die Kreuzreaktivität des Strongstep®-Systemgeräts SARS-COV-2-Antigen-Schnelltest wurde bewertet, indem verschiedene Mikroorganismen (10⁶ CFU/ml), Viren (10⁵ PFU/ml) und negative Matrixen getestet wurden, die möglicherweise mit dem StrongStep® gekreuzt werden können Systemgerät SARS-COV-2-Antigen-Schnelltest.
Jeder Organismus und jeder Virus wurden dreifach getestet. Basierend auf den in dieser Studie generierten Daten ist das Strongstep®-Systemgerät für den SARS-CoV-2-Antigen-Rap-Test nicht mit den getesteten Organismen oder Viren gekreuzt.
c) Substanz interferieren:
Mögliche störende Substanzen des Strongstep® SARS-COV-2-Antigen-Schnelltests wurden bewertet, indem verschiedene Substanzen mit der Konzentration unten getestet wurden, die möglicherweise den Strongstep® SARS-COV-2-Antigen-Schnelltest stören. Jede Substanz wurde dreifach getestet. Basierend auf den in dieser Studie generierten Daten stört der Strongstep® SARS-CoV-2-Antigen-Rapid-Test die getesteten Substanzen nicht.
d) Hakeneffekt
Die höchste Konzentration an hitzeinaktivierten SARS-CoV-2-Bestands (TCID)50von 5,00 x 105/ml) wurde getestet. Es wurde kein Hakeneffekt erkannt.




1人份抗原卡实物图唾液版1_00_副本-300x216.png)